Oncologie
C.1 Botmetastasen
Aanbevelingen
Ga na bij de verwijzer of er sprake is van stabiele botmetastasen. Verzamel in aanvulling daarop zoveel mogelijk informatie die van belang is voor de fysio- of oefentherapeutische behandeling; in het bijzonder in verband met het risico op het optreden van een (pathologische) fractuur of compressie van het ruggenmerg.
Deze informatie behelst minimaal:
- de locatie en aard van de botmetastasen (zo gedetailleerd mogelijk);
- de aanwezigheid van neurologische symptomen;
- de aanwezigheid van osteoporose;
- de aanwezigheid van pijn die is gerelateerd aan de locatie van metastasen;
- eerdere fracturen;
- de behandeling die is ingezet vanwege de botmetastasen;
- de inschatting van het valrisico.
Beoordeel deze informatie periodiek opnieuw.
Kom in samenspraak met de behandelend arts of verpleegkundig specialist tot een geschikt oefen- of fysiotherapeutisch behandelplan.
Weeg voor de start van een beweeginterventie in samenspraak met de patiënt de voor- en nadelen tegen elkaar af. Betrek daar het volgende bij:
- de risico’s van de beweeginterventie die door de arts zijn benoemd (zoals het risico op fracturen of compressie van het ruggenmerg);
- de mate waarin de beweeginterventie kan worden aangepast om de risico’s te minimaliseren;
- potentiële voordelen van de beweeginterventie en de gezondheidsrisico’s van niet bewegen, zoals het valrisico dat voortkomt uit inactiviteit en het daarmee gepaard gaande verhoogde risico op fracturen.
Bied de beweeginterventie gepersonaliseerd aan en houd rekening met de locatie en aard van de botmetastasen. Stem de manier waarop bewegingen worden uitgevoerd af op de locatie van de botmetastasen indien dit nodig is.
Bied de beweeginterventie bij voorkeur gesuperviseerd aan bij patiënten met botmetastasen. Instrueer patiënten die de voorkeur geven aan zelfstandig trainen, ten minste over de manier waarop de oefeningen veilig en effectief kunnen worden uitgevoerd.
Vermijd dwarse krachten en/of compressiekrachten op een locatie met aangetoonde metastasen om het risico op een fractuur te verminderen. Dit geldt ook voor de uitvoering van inspanningsdiagnostiek.
Pas bij voorkeur een beweeginterventie toe waarbij zoveel mogelijk functioneel wordt getraind. Overweeg bij deze training het eigen lichaamsgewicht (zwaartekracht) te gebruiken in plaats van apparatuur en halters. Formuleer samen met de patiënt heldere doelen en communiceer verwachtingen.
Ga niet over tot begeleiding van patiënten met instabiele botmetastasen zonder dat er een uitgebreide risicobeoordeling heeft plaatsgevonden in overleg met de betrokken arts en eventueel andere betrokken behandelaars.
Bied bij patiënten met instabiele botmetastasen een oefenprogramma of beweeginstructies aan met een focus op functioneel oefenen binnen de grenzen zoals afgesproken in een multidisciplinair team.
Aanleiding
Botmetastasen kunnen leiden tot pijn, een afname van fysieke functies en verminderd functioneren op het gebied van activiteiten en participatie. Als gevolg hiervan kunnen patiënten met botmetastasen een afname in kwaliteit van leven ervaren. Voldoende fysieke activiteit en lichaamsbeweging kunnen zorgen voor een verbetering van het lichamelijk functioneren en worden aanbevolen voor mensen die leven met of na kanker. Voor patiënten met botmetastasen blijft een beweeginterventie vaak onbenut door onzekerheid over de veiligheid en het risico op bijwerkingen, zoals pathologische fracturen. Om therapeuten te ondersteunen, is het daarom belangrijk om aanbevelingen te formuleren voor het veilig toepassen van effectieve beweeginterventies in aanwezigheid van botmetastasen.
Uitgangsvraag
Wat is een veilige toepassing van beweeginterventies bij patiënten met botmetastasen?
Literatuur
In de literatuur is beschreven dat beweeginterventies voor patiënten met stabiele botmetastasen geen verhoogd risico geven op ernstige bijwerkingen als gevolg van een beweeginterventie in vergelijking met geen beweeginterventie. Zelfs deelname aan sport en spelvormen wordt in verband gebracht met een zeer laag risico op bijwerkingen die zijn gerelateerd aan het bewegen in aanwezigheid van stabiele botmetastasen.
In een groot deel van de wetenschappelijke studies zijn patiënten met pijn of instabiele botmetastasen echter niet geïncludeerd en was voor deelname aan een beweeginterventie toestemming van de behandelend arts, een uitgebreide overdracht met de functionele status van de patiënt of een minimumniveau van functioneren nodig.
In aanwezigheid van botmetastasen werden krachtoefeningen voorgeschreven waarbij de belasting van het gebied met botmetastasen geminimaliseerd werd en/of werden weerstandsbanden gebruikt in plaats van apparaten. Met deze aanpassingen zijn bij patiënten met botmetastasen alsnog positieve effecten gevonden op verschillende uitkomsten, zoals fysiek functioneren en spierkracht.
Overwegingen
Wanneer wordt overwogen een beweeginterventie aan te bieden aan patiënten met botmetastasen is het belangrijk om de juiste achtergrondinformatie te verzamelen. Patiënten die met botmetastasen bij een therapeut komen, zullen in de meeste gevallen te maken hebben met stabiele metastasen. Bij twijfel is het belangrijk dit te verifiëren bij de behandelend arts. In het volgende kader is een overzicht opgenomen van mogelijke risicofactoren. Deze lijst is opgesteld door een internationale werkgroep die bestaat uit experts op het gebied van bewegen bij botmetastasen, op grond van systematisch literatuuronderzoek en raadpleging van stakeholders (Campbell 2022, Weller 2021). Op basis van deze risicofactoren kan de therapeut beoordelen of de focus van een beweeginterventie voornamelijk op beweegvoorbereiding komt te liggen (gericht op juiste, veilige uitvoering van beweging), op oefening of op training. Zie de volgende figuur.
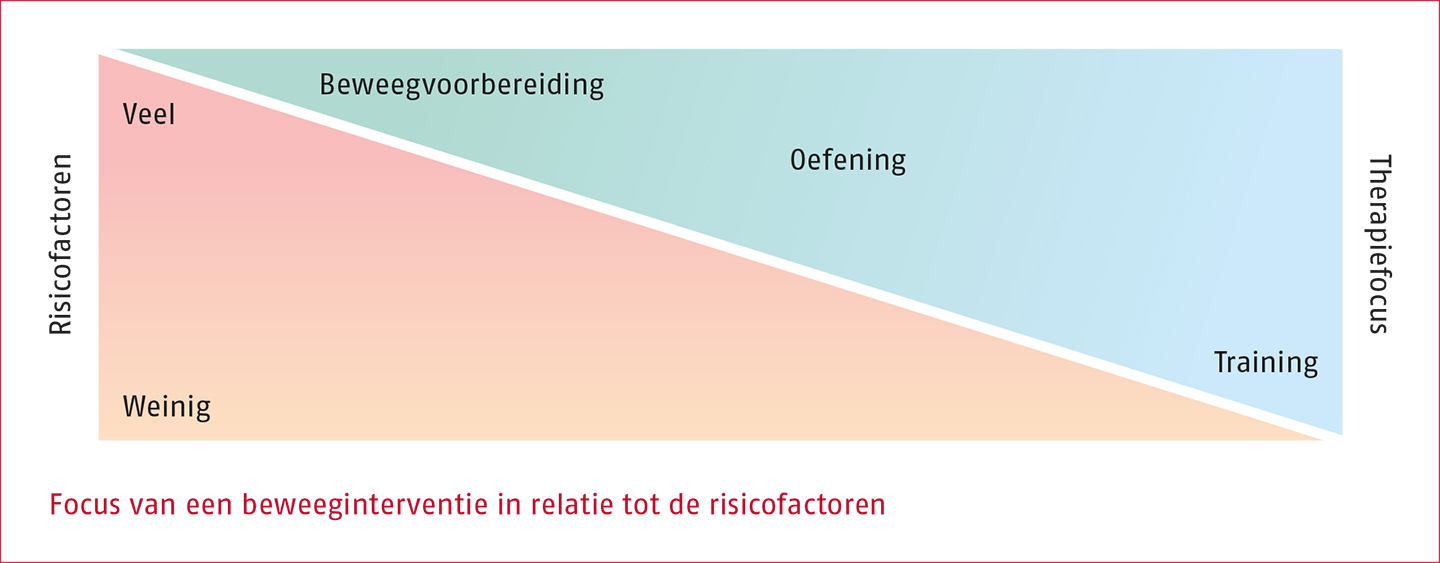
Risicofactoren voor bewegen bij patiënten met botmetastasen
Osteolytische metastasen
- Metastasen in gewichtdragende botten (femur, wervelkolom, bekkenring, heupkom)
- Pijn gerelateerd aan de locatie van metastasen
- Neurologische symptomen
- Gebruik van pijnmedicatie gerelateerd aan de locatie van metastasen
Aan de behandeling van metastasen gerelateerde factoren
- Bestraling van de metastasen in de afgelopen twee maanden
- Geplande of eerdere chirurgische of medische behandeling voor skeletgerelateerde voorvallen of symptomatische aandoeningen die zijn gerelateerd aan het skelet
Aan (de behandeling van) kanker gerelateerde factoren
- Progressie van de ziekte
- Metastasen in andere orgaansystemen (bijvoorbeeld hersenen, long)
- Type kanker dat zich vaak uit in osteolytische metastasen (zoals long-, schildklier- en niercelcarcinoom)
- Huidig gebruik van medicatie die de afbraak van botten remt of botten steviger maakt (denosumab, zoledroninezuur), of gebruik gedurende een periode > 6 maanden
Aan de patiënt gerelateerde factoren
- Algemene symptomen zoals comorbiditeit, vermoeidheid, extreem gewichtsverlies
- Geen of weinig ervaring met lichaamsbeweging
- Slechte ECOG-prestatiestatus
- Twee of meer valpartijen in de afgelopen 12 maanden
- Osteoporose
- Beperkingen in ADL
- Cognitieve stoornissen die het naleven van voorzorgsmaatregelen
ECOG = 'Eastern Cooperative Oncology Group'
Daarnaast kan in het geval van metastasen in lange pijpbeenderen een risicoanalyse gemaakt worden met behulp van de ‘Mirels Classification’ (Howard 2018; Sheill 2018) en bij metastasen in de wervelkolom met de ‘Spinal Instability Neoplastic Score’ (SINS; Fox 2017). Deze scores worden echter niet in alle Nederlandse ziekenhuizen routinematig gebruikt, en zijn dus niet altijd voorhanden. Neurologische symptomen zijn verdacht en de therapeut verwijst de patiënt met neurologische symptomen altijd direct terug naar de arts voor aanvullend onderzoek.
Bij het inrichten van de beweeginterventie houdt de therapeut rekening met de locatie en aard van de botmetastase(n), om het risico te verlagen. Als er aanpassingen nodig zijn, kan gedacht worden aan het weglaten van bepaalde oefeningen of tests, het minder belasten van een bepaald gebied of het aanpassen van een beweging, oefening of test. Door Galvão (2011) is een multimodale beweeginterventie opgesteld voor patiënten met prostaatkanker en botmetastasen om compressiebelasting op de gebieden met botmetastasen te minimaliseren en rekening te houden met verminderde belastbaarheid van het bot. Zie de volgende tabel. 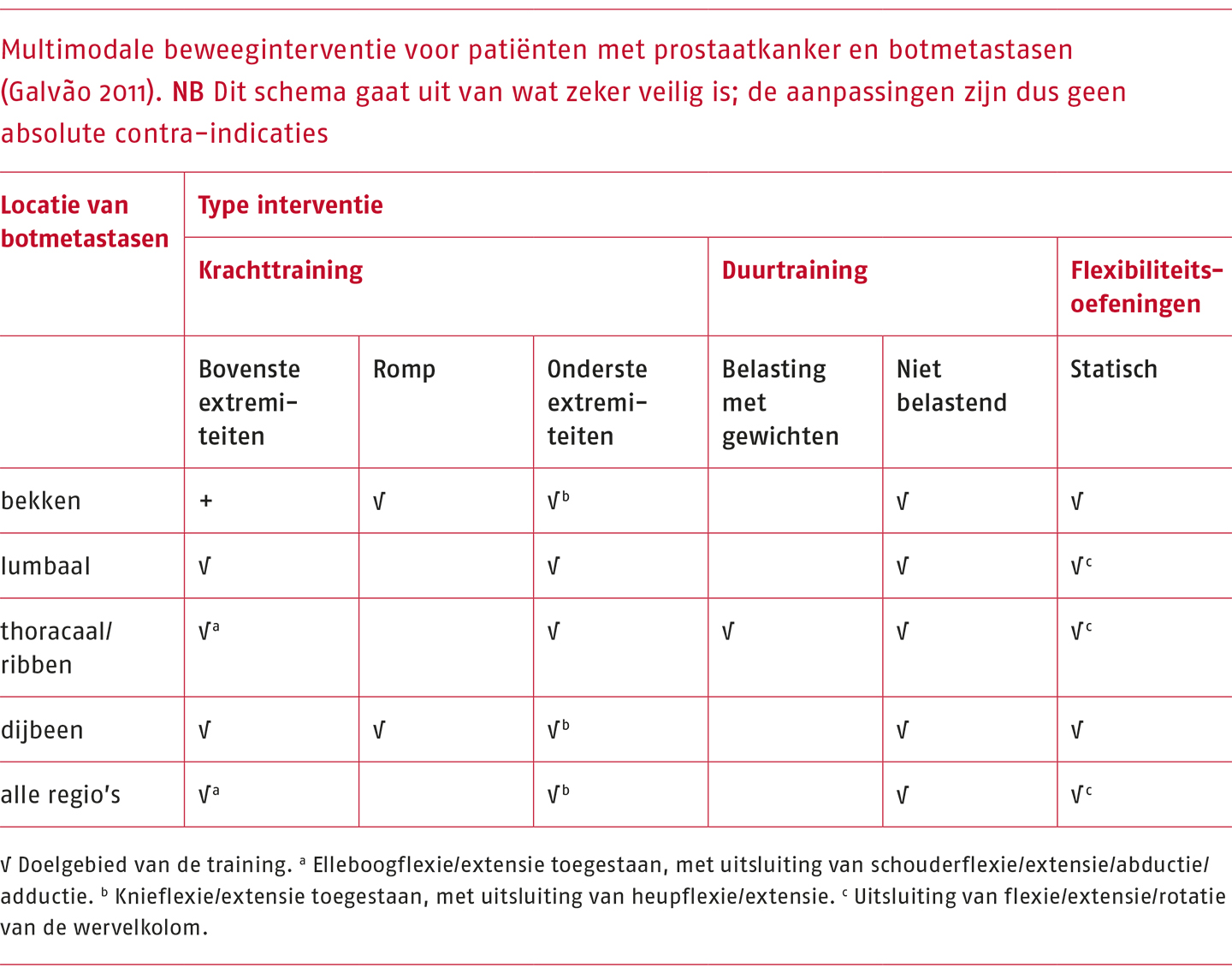
De therapeut hoort zich zo min mogelijk te laten leiden door beperkingen, maar moet zich realiseren dat bepaalde oefeningen een verhoogd risico met zich meebrengen, bijvoorbeeld bij dwarse krachten op een locatie met aangetoonde metastasen. Directe 1RM-tests worden afgeraden. Bij stabiele botmetastasen worden 12 RM-tests over het algemeen veilig geacht. Er kan ook overwogen worden geen tests uit te voeren en de belasting pragmatisch te bepalen op grond van ervaren belasting en kwaliteit van uitvoering van de beweging. Daarom is het belangrijk dat de therapeut bij elke oefening een analyse maakt van de keten van krachtoverbrenging, en hoe als gevolg hiervan de aangedane regio wordt belast (Guo 2020). Hierbij wordt rekening gehouden met afwijkende beweegpatronen ten gevolge van bewegingsangst. Deze kunnen potentieel klachten in andere gebieden opleveren. De patiënt een beweeginterventie onthouden kan indirect ook tot schade leiden, doordat inactiviteit kan leiden tot vallen en een verhoogd risico op fracturen.
Functioneel trainen is bij patiënten met botmetastasen belangrijk. Mogelijk verlaagt functioneel trainen het risico van een beweeginterventie, omdat daarbij alleen het eigen gewicht, de zwaartekracht en functionele gewichten worden gebruikt, die de patiënt in het dagelijks leven ook zou gebruiken. De therapeut moedigt de patiënt aan om te bewegen, en geeft een goede uitleg over eventuele risico’s en hoe deze zoveel mogelijk kunnen worden beperkt. Hierbij kan gedacht worden aan het aanpassen van de manier waarop de diverse bewegingen kunnen worden uitgevoerd, daar waar dat nodig is. Kennisoverdracht tussen therapeut en patiënt over hoe en in welke vorm bewegingsopdrachten worden uitgevoerd is belangrijk, alsmede communicatie tussen betrokken zorgverleners onderling zodat de patiënten een eenduidig advies krijgt, om er zeker van te zijn dat alle relevante informatie over de (belastbaarheid van) botmetastasen bekend is bij alle betrokken zorgverleners, en om ervoor te zorgen dat symptomen en verschijnselen die mogelijk gerelateerd zijn aan (verergering van) botmetastasen tijdig worden opgemerkt.
Over het algemeen zijn de risico’s van een beweeginterventie bij patiënten met stabiele botmetastasen laag, maar deze eventuele risico’s op fracturen of compressie van het ruggenmerg, zoals aangegeven door de arts, worden wel met de patiënt besproken, toegelicht en vastgelegd in het dossier. De therapeut weegt deze risico’s in samenspraak met de patiënt af tegen de voordelen van bewegen en de risico’s van niet bewegen.
De wetenschappelijke evidentie over veiligheid en haalbaarheid van beweeginterventies bij patiënten met instabiele botmetastasen is beperkt. De begeleiding bij patiënten met instabiele botmetastasen verschilt van patiënt tot patiënt en vraagt een uitgebreide risicobeoordeling en overleg met de betrokken zorgverleners.
Wanneer een patiënt met botmetastasen zelfstandig wil trainen, is het noodzakelijk dat de therapeut de patiënt instrueert in het veilig uitvoeren van oefeningen. Op enig moment en op enig niveau zal (periodieke) supervisie belangrijk zijn. Afhankelijk van de situatie van de patiënt maakt de therapeut een inschatting van de frequentie waarop de patiënt wordt gezien.
Zoekactie
De informatie die nodig is voor het formuleren van aanbevelingen ten aanzien van de veiligheid van beweeginterventies bij patiënten met botmetastasen is vergaard met behulp van het recentelijk uitgevoerd systematisch literatuuronderzoek van Weller (2021). In dit onderzoek worden onder andere de veiligheid, haalbaarheid en effectiviteit beschreven van beweeginterventies bij patiënten met botmetastasen op basis van de evidentie van gecontroleerde studies. Het literatuuronderzoek is uitgevoerd op 16 juli 2020 in de elektronische databases MEDLINE, Embase, PubMed CINAHL, PEDro en CENTRAL.
De selectiecriteria die Weller (2021) hanteerde, zijn opgenomen in de volgende tabel.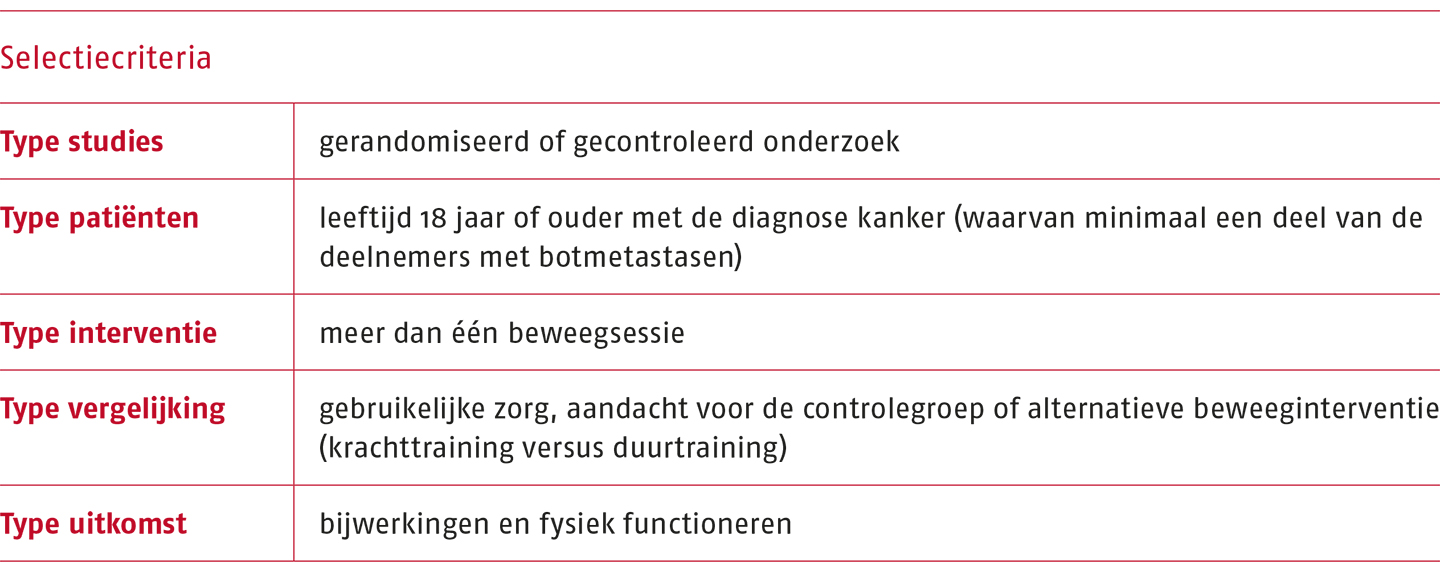
Karakteristieken van geïncludeerde studies
In totaal zijn 16 studies geïncludeerd waarin de haalbaarheid en effectiviteit van krachttraining (5 studies), duurtraining (1 studie), een combinatie van kracht- en duurtraining (7 studies) of een beweeginterventie in spelverband (3 studies) zijn onderzocht in zowel een gesuperviseerde als een niet-gesuperviseerde setting. Daarnaast is één studie geïncludeerd waarin de effectiviteit van kracht- en duurtraining met elkaar is vergeleken. 13 studies includeerden zowel patiënten met als zonder botmetastasen en vier studies includeerden alleen patiënten met botmetastasen. Van de 1489 deelnemers die zijn geïncludeerd in de review, hadden er 645 (43%) botmetastasen; de gemiddelde leeftijd van de deelnemers was 65 jaar. Op basis van de gegevens van drie studies varieerde de leeftijd van 32 tot 87 jaar. Negen studies onderzochten de effectiviteit van een gesuperviseerde beweeginterventie; in zes studies werd een combinatie van gesuperviseerde en niet-gesuperviseerde sessies aangeboden en in twee studies bestond de interventie uit niet-gesuperviseerde sessies. De supervisie werd verzorgd door gekwalificeerde fysiotherapeuten, inspanningsfysiologen of sportprofessionals.
Negen studies rapporteerden bijwerkingen in zowel de interventie- als de controlegroep, zeven studies alleen in de interventiegroep en één studie rapporteerde helemaal geen bijwerkingen, maar alleen vermoeidheidsklachten. Zeven studies gebruikten een classificatietool om de ernst van de bijwerkingen te beoordelen. In drie studies werden ernstige bijwerkingen gerapporteerd van zowel patiënten met als zonder botmetastasen. Van de 57 ernstige bijwerkingen traden er 27 op in de interventie- en 30 in de controlegroep. Vier ernstige bijwerkingen (in 0,5% van het totaal aantal deelnemers aan de beweeginterventie) konden worden toegeschreven aan de beweeginterventie. Alle bijwerkingen konden worden toegeschreven aan een voetbaltraining en traden niet op in het gebied met de botmetastasen. De ernstige bijwerkingen bestonden uit: twee fracturen, één achillespeesruptuur en één infectie als gevolg van een schram die werd veroorzaakt door een scheenbeschermer. In de vier studies waarin alleen patiënten met botmetastasen werden geïncludeerd, zijn geen ernstige bijwerkingen gerapporteerd.
In negen studies werden geen patiënten geïncludeerd met pijn of instabiele botmetastasen. Ook was voor deelname aan vier studies toestemming van de arts noodzakelijk en in acht studies was een minimale prestatiestatus vereist (‘Eastern Cooperative Oncology Group’ (ECOG) prestatiestatus 0-1/2; Karnofsky-prestatiestatus (KPS) > 70). Daarnaast werden in zeven van de geïncludeerde studies de trainingsvoorschriften aangepast in verband met de botmetastasen. Zo werden krachtoefeningen voorgeschreven waarbij de belasting van het gebied met botmetastasen geminimaliseerd werd, en/of werden weerstandsbanden gebruikt in plaats van apparaten.
In geen van de 17 studies werden significant negatieve effecten gerapporteerd. Ten opzichte van de controlegroep werd in zeven studies een significante verbetering in fysiek functioneren gerapporteerd, in drie studies een significante vermindering in vermoeidheid en vier studies rapporteerden een significante verbetering in kwaliteit van leven als gevolg van de beweeginterventie. Zes studies rapporteerden een significante verbetering in lichaamssamenstelling en objectief gemeten spierkracht. In twee studies werd een significante vermindering van pijn gerapporteerd als gevolg van de beweeginterventie. In de vier studies waarin alleen patiënten met botmetastasen waren geïncludeerd, werd geen significant effect op vermoeidheid of kwaliteit van leven gevonden. Wel werd een significante verbetering in fysiek functioneren (3 studies) en spierkracht (2 studies) gerapporteerd. Eén studie rapporteerde daarnaast een significante vermindering in pijn als gevolg van de beweeginterventie, terwijl in drie studies geen verschil in pijn tussen de interventie- en de controlegroep werd gevonden.
Individuele studiekwaliteit
De opzet en uitvoering van de individuele studies (‘risk of bias’; RoB) zijn in de meta-analyse van Weller (2021) beoordeeld met behulp van de ‘Cochrane Risk of Bias 2.0’. Voor de beoordeling van de studie van Rosenberger (2017) is gebruikgemaakt van ‘Risk of Bias In Non-Randomized Studies of Interventions’ (ROBINS). Zie voor de beoordeling van de RoB van alle individuele studies die Weller includeerde bijlage C.1-1.
Kwaliteit van de gevonden literatuur
Een van de items van de RoB-tool beschrijft waarin is afgeweken van de voorgeschreven interventie. Omdat de beschrijving van dit item als onduidelijk is beoordeeld in acht van de 17 studies (47%) en die onduidelijkheid mogelijk invloed heeft gehad op de gevonden resultaten, is de bewijskracht van de meta-analyse met één niveau verlaagd. Dit had tot gevolg dat de kwaliteit van het bewijs als redelijk is beoordeeld. Zie voor het GRADE-evidenceprofiel de volgende tabel.
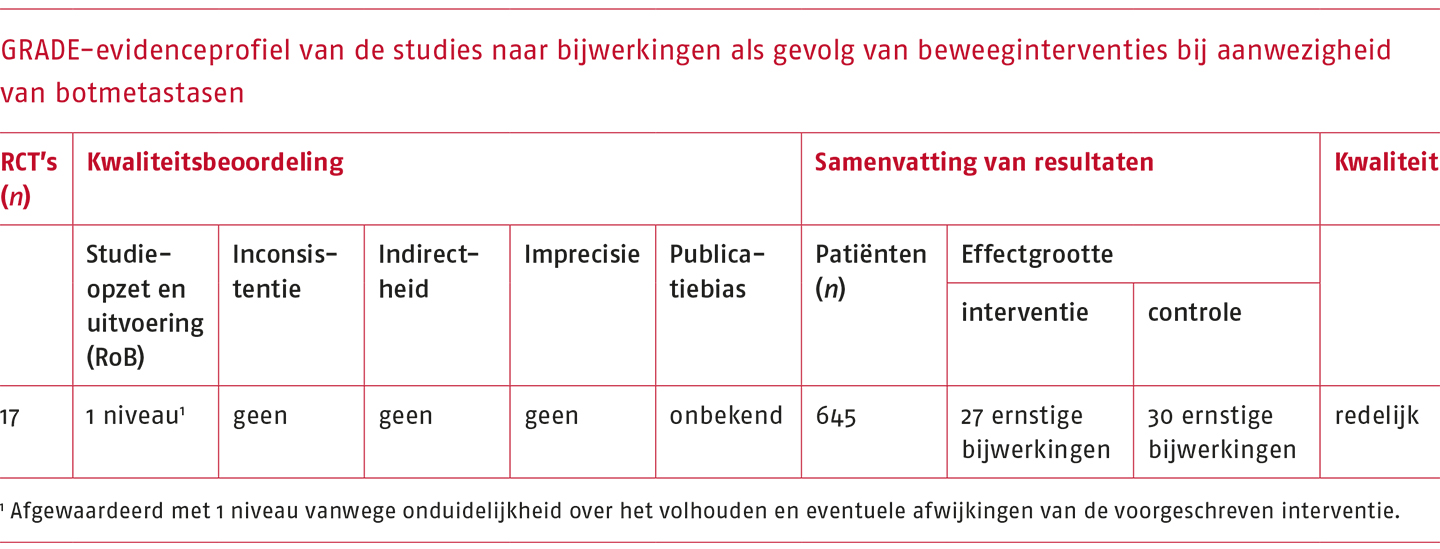
Conclusie op basis van de literatuur
Er is bewijs van redelijke kwaliteit dat beweeginterventies bij patiënten met stabiele botmetastasen niet leiden tot een verhoogd risico op ernstige bijwerkingen in vergelijking met geen beweeginterventie, maar alleen als de beweeginterventie aangepast wordt aan de locatie van botmetastasen.
Overwegingen
De aanbevelingen worden niet alleen bepaald door bevindingen in de literatuur. Ook andere overwegingen spelen daarbij een rol. De overwegingen betroffen:
Gewenste effecten: Bij patiënten met botmetastasen kan een beweeginterventie belangrijke voordelen opleveren op de uitkomstmaten, zoals op fysiek functioneren en op spierkracht.
Ongewenste effecten: Het risico op ernstige bijwerkingen als gevolg van een beweeginterventie bij patiënten met botmetastasen is zeer klein, maar alleen als de beweeginterventie wordt aangepast aan de locatie van de botmetastasen. De evidentie beperkt zich tot stabiele metastasen. Bij instabiele metastasen is een uitgebreide risicobeoordeling nodig, evenals overleg met de betrokken zorgverleners.
Kwaliteit gewenste effecten: De bewijskracht is redelijk.
Balans tussen gewenste en ongewenste effecten: Aangezien er geen aanwijzingen zijn dat een beweeginterventie bij patiënten met stabiele botmetastasen ook maar enige mate leidt tot een verhoogd risico, maar mogelijk wel effectief is ter verbetering van fysiek functioneren en spierkracht, overstijgen de gewenste de ongewenste effecten. De risico’s van de beweeginterventie moeten in gezamenlijkheid met de patiënt afgewogen worden tegen de voordelen van bewegen en de gezondheidsrisico’s van niet bewegen.
Waarde aan gewenste effecten: Het onthouden van een effectieve beweeginterventie kan tot schade leiden. Een voorbeeld daarvan is dat het valrisico zal toenemen door inactiviteit. Het onthouden van een effectieve interventie kan daardoor leiden tot een toename van vallen en daarmee het risico op fracturen. Het belang van een voor de patiënt toereikende conditie en een goede uitvoer van beweging is duidelijk in verband met het optimaliseren van activiteiten van het dagelijks leven, het algemeen welbevinden van de patiënt, het verkleinen van het valrisico en het durven bewegen ondanks de botmetastasen.
Variatie in waarde aan gewenste effecten: De effectiviteit en veiligheid van beweeginterventies bij patiënten met instabiele botmetastasen zijn onbekend. Begeleiding bij patiënten met botmetastasen verschilt van patiënt tot patiënt. Bij instabiele botmetastasen verdient de begeleiding extra aandacht in verband met het verhoogde risico op incidenten.
Benodigde middelen (kosten): Er zijn geen extra kosten verbonden aan de interventie (ten opzichte van reguliere behandeling door de fysio- of oefentherapeut).
Variatie in benodigde middelen (kosten): Niet van toepassing.
Kosteneffectiviteit: Er is geen evidentie beschikbaar over de kosteneffectiviteit van een beweeginterventie bij patiënten met botmetastasen.
Aanvaardbaarheid: Bij aanwezigheid van stabiele botmetastasen moet bewegen zoveel mogelijk worden aangemoedigd. Begeleiding van patiënten met instabiele botmetastasen vereist een uitgebreide risicobeoordeling in overleg met de betrokken arts en eventueel andere betrokken behandelaars. Om te komen tot risicoreductie, in geval er sprake is van risico’s, kan zoveel mogelijk functioneel worden getraind, waarbij alleen gebruik wordt gemaakt van het eigen gewicht, de zwaartekracht en functionele gewichten die de patiënt in het dagelijks leven ook zou gebruiken. Artsen, verpleegkundigen of verpleegkundig specialisten zouden bedenkingen kunnen uiten over de veiligheid van de belasting bij patiënten. Het is essentieel dat tussen alle betrokken behandelaars op grond van expliciete klinische overwegingen overeenstemming is over wat veilig kan en wat niet, zodat aan de patiënt een eenduidig advies kan worden gegeven en de patiënt niet aan onnodige risico’s wordt blootgesteld, maar ook geen effectieve zorg wordt onthouden.
Haalbaarheid: De implementatie van beweeginterventies bij patiënten met stabiele botmetastasen is in de dagelijkse praktijk haalbaar in een eerstelijnspraktijk, waarbij goede informatie van de behandelend arts over de aard en de locatie van de botmetastasen essentieel is. De therapeut hoort zich zo min mogelijk te laten leiden door beperkingen, maar moet zich wel realiseren dat bepaalde oefeningen risicoverhogend kunnen werken (bijvoorbeeld: dwarse krachten of compressiekrachten op een locatie met aangetoonde metastasen). Om een juiste risico-inschatting te maken, is het noodzakelijk om van de behandelend arts informatie te krijgen over de locatie van de metastasen en deze informatie te gebruiken bij het beoordelen van de veiligheid van oefentherapie en training. De therapeut gaat bij de verwijzer na of er sprake is van stabiele of instabiele metastasen en of er sprake is van neurologische symptomen, osteoporose, pijn die is gerelateerd aan de locatie van de metastasen, eerdere fracturen, welke behandeling is ingezet vanwege de botmetastasen en hoe het valrisico wordt ingeschat. Op basis van deze risicofactoren kan, in samenspraak met de behandelend arts of verpleegkundig specialist, tot een geschikt fysio- of oefentherapeutisch behandelplan gekomen worden. De informatie die de therapeut verzamelt is in overleg met de werkgroep en de klankbordgroep geselecteerd en sluit aan bij op dit moment in ontwikkeling zijnde internationale richtlijnen. De aard van de botmetastasen is in deze overweging opgenomen in verband met een mogelijk groter risico op fracturen bij osteolytische metastasen dan bij osteoblastische metastasen of gemengd osteolytische/osteoblastische metastasen.
Conclusie
De werkgroep adviseert zoveel mogelijk relevante informatie te verzamelen, en in samenspraak met de behandelend arts of verpleegkundig specialist tot een geschikt fysio- of oefentherapeutisch behandelplan te komen.
Meetinstrumenten
Botmetastasen zijn vooral aanwezig in sterk doorbloede gedeeltes van het bot, zoals de wervelkolom, het bekken en de lange pijpbeenderen. Bij 70% van de patiënten zijn de botmetastasen afkomstig van een mamma-, long-, prostaat-, schildklier- of niercelcarcinoom. Bij ongeveer 70% van de patiënten met botmetastasen bestaan de symptomen uit botpijn en verminderde mobiliteit. Botmetastasen kunnen zichtbaar worden gemaakt met behulp van een röntgenfoto, MRI, botscintigrafie of CT-scan. Eventueel kan behalve radiologisch onderzoek een biopsie worden uitgevoerd wanneer er nog geen eerder bewezen botmetastasen zijn geïdentificeerd. De diagnostiek van botmetastasen zal daarom altijd door een arts worden uitgevoerd. Bij de intake voor een beweeginterventie zal een eventuele beperking of bedreiging van het inspanningsvermogen in kaart moeten worden gebracht. Bij het selecteren van meetinstrumenten voor het meten van de inspanningscapaciteit en andere functies van het bewegingsapparaat houdt de fysio- of oefentherapeut rekening met de locatie en aard van de botmetastasen, op vergelijkbare wijze als bij het aanbieden van training. Het toepassen van directe 1RM-tests wordt afgeraden. De therapeut consulteert bij twijfel over de uitvoering van een beweeginterventie bij patiënten met botmetastasen de primaire behandelaar.
Het evidence-to-decisionformulier voor de veilige toepassing van beweeginterventies bij patiënten met botmetastasen is opgenomen als bijlage C.1-2.
- Bjerre ED, Brasso K, Jørgensen AB, Petersen, TH, Eriksen AR, Tolver A, Christensen JF, Poulsen MH, Madsen SS, Østergren PB, Borre M, Krustrup P, Johansen C, Rørth M, Midtgaard J. Football compared with usual care in men with prostate cancer (FC Prostate Community Trial): a pragmatic multicentre randomized controlled trial. Sports Med. 2019;49(1):145-58.
- Bourke L, Doll H, Crank H, Daley A, Rosario D, Saxton JM. Lifestyle intervention in men with advanced prostate cancer receiving androgen suppression therapy: a feasibility study. Cancer Epidemiol Biomarkers Prev. 2011;20(4):647-57.
- Bourke L, Gilbert S, Hooper R, Steed LA, Joshi M, Catto JWF, Saxton JM, Rosario DJ. Lifestyle changes for improving disease-specific quality of life in sedentary men on long-term androgen-deprivation therapy for advanced prostate cancer: a randomised controlled trial. Eur Urol. 2014;65(5):865-72.
- Campbell KL, Cormie P, Weller S, Alibhai SMH, Bolam KA, Campbell A, Cheville AL, Dalzell MA, Hart NH, Higano CS, Lane K, Mansfield S, McNeely ML, Newton RU, Quist M, Rauw J, Rosenberger F, Santa Mina D, Schmitz KH, Winters-Stone KM, Wiskemann J, Goulart J. Exercise Recommendation for People with Bone Metastases: Expert Consensus for Health Care Providers and Exercise Professionals. JCO. 2022; online ahead of print.
- Cheville AL, Moynihan T, Herrin J, Loprinzi C, Kroenke K. Effect of collaborative telerehabilitation on functional impairment and pain among patients with advanced-stage cancer: a randomized clinical trial. JAMA Oncol. 2019;5(5):644-52.
- Cormie P, Newton RU, Spry N, Joseph D, Taaffe DR, Galvao DA. Safety and efficacy of resistance exercise in prostate cancer patients with bone metastases. Prostate Cancer Prostatic Dis. 2013;16(4):328-35.
- Dawson JK, Dorff TB, Todd Schroeder E, Lane CJ, Gross ME, Dieli-Conwright CM. Impact of resistance training on body composition and metabolic syndrome variables during androgen deprivation therapy for prostate cancer: a pilot randomized controlled trial. BMC Cancer. 2018;18(1):368.
- Fox S, Spiess M, Hnenny L, Fourney DR. Spinal Instability Neoplastic Score (SINS): reliability among spine fellows and resident physicians in orthopedic surgery and neurosurgery. Global Spine J. 2017;7(8):744-48.
- Galvão DA, Taaffe DR, Spry N, Cormie P, Joseph D, Chambers SK, Chee R, Peddle-McIntyre CJ, Hart NH, Baumann FT, Denham J, Baker M, Newton RU. Exercise preserves physical function in prostate cancer patients with bone metastases. Med Sci Sports Exerc. 2018;50(3):393-9.
- Guo Y, Ngo-Huang AT, Fu JB. Perspectives on spinal precautions in patients who have cancer and spinal metastasis. Phys Ther. 2020. 100(3):554-63.
- Howard EL, Shepherd KL, Cribb G, Cool P. The validity of the Mirels score for predicting impending pathological fractures of the lower limb. Bone Joint J. 2018;8(8):1100-05.
- Integraal Kankercentrum Nederland (IKNL). Richtlijn botmetastasen. Utrecht: IKNL; 2010. Geraadpleegd op 11 mei 2021. Beschikbaar via https://richtlijnendatabase.nl/
- Litterini AJ, Fieler VK, Cavanaugh JT, Lee JQ. Differential effects of cardiovascular and resistance exercise on functional mobility in individuals with advanced cancer: a randomized trial. Arch Phys Med Rehabil. 2013;94(12):2329-35.
- Rief H, Petersen LC, Omlor G, Akbar M, Bruckner T, Rieken S, Haefner MF, Schlampp I, Förster R, Debus J, Welzel T, German Bone Research Group. The effect of resistance training during radiotherapy on spinal bone metastases in cancer patients - a randomized trial. Radiother Oncol. 2014;112(1):133-9.
- Rosenberger F, Wiskemann J, Vallet S, Haag GM, Schembri E, Jäger D, Grüllich C. Resistance training as supportive measure in advanced cancer patients undergoing TKI therapy-a controlled feasibility trial. Support Care Cancer. 2017;25(12):3655-64.
- Scott JM, Zabor EC, Schwitzer E, Koelwyn GJ, Adams SC, Nilsen TS, Moskowitz CS, Matsoukas K, Iyengar NM, Dang CT, & Jones LW. Efficacy of Exercise Therapy on Cardiorespiratory Fitness in Patients With Cancer: A Systematic Review and Meta-Analysis. J Clin Oncol. 2018;36(22):2297-305.
- Sheill G, Guinan EM, Peat N, Hussey J. Considerations for exercise prescription in patients with bone metastases: a comprehensive narrative review. PM R. 2018;10(8):843-6.
- Solheim TS, Laird BJA, Balstad TR, Stene GB, Bye A, Johns N, Pettersen CH, Fallon M, Fayers P, Fearon K, Kaasa S. A randomized phase II feasibility trial of a multimodal intervention for the management of cachexia in lung and pancreatic cancer. J Cachexia Sarcopenia Muscle. 2017;8(5):778-88.
- Sprave T, Rosenberger F, Verma V, Förster R, Bruckner T, Schlampp I, Bostel T, Welzel T, Akbaba S, Rackwitz T, Nicolay NH, Grosu AL, Wiskemann J, Debus J, Rief H. Paravertebral muscle training in patients with unstable spinal metastases receiving palliative radiotherapy: an exploratory randomized feasibility trial. Cancer (Basel). 2019;11(11):1771.
- Uster A, Ruehlin M, Mey S, Gisi D, Knols R, Imoberdorf R, Pless M, Ballmer PE. Effects of nutrition and physical exercise intervention in palliative cancer patients: A randomized controlled trial. Clin Nutr. 2018;37(4):1202-9.
- Uth J, Hornstrup T, Schmidt JF, Christensen JF, Frandsen C, Christensen KB, Helge EW, Brasso K, Rørth, Midtgaard J, Krustrup P. Football training improves lean body mass in men with prostate cancer undergoing androgen deprivation therapy. Scand J Med Sci Sports. 2014;24 Suppl 1:105-12.
- Villumsen BR, Jorgensen MG, Frystyk J, Hørdam B, Borre M. Home-based ‘exergaming’ was safe and significantly improved 6-min walking distance in patients with prostate cancer: a single-blinded randomised controlled trial. BJU Int. 2019 Apr 22. Published ahead of print. Doi: 10.1111/bju.14782
- Weller S, Hart NH, Bolam KA, Mansfield S, Santa Mina D, Winters-Stone KM, Campbell A, Rosenberger F, Wiskemann J, Quist M, Cormie P, Goulart J, Campbell KL. Exercise for individuals with bone metastases: A systematic review. Crit Rev Oncol Hematol. 2021 Oct;166:103433.
- Yee J, Davis GM, Hackett D, Beith JM, Wilcken N, Currow D, Emery J, Philips J, Martin A, Hui R, Harrison M, Segelov E, Kilbreath SL. Physical activity for symptom management in women with metastatic breast cancer: a randomized feasibility trial on physical activity and breast metastases. J Pain Symptom Manage. 2019;58(6):929-39.
